高中化学教材中关于《乙炔的制取实验》有两点令人不满的:一、碳化钙与水反应太快,并有大量泡沫,不易控制。点燃乙炔气时产生大量黑烟漂浮在教室里,在做后面的几个乙炔性质实验时,几乎没有乙炔气排出了。二、把纯净的乙炔气体通入高锰酸钾酸性溶液和溴的四氯化碳溶液里,都能发生退色反应。可是却没说明净化乙炔气体的方法,所以,多数教师把电石与水反应生成的乙炔气直接通入上述两种溶液里,都迅速发生了退色反应,因为用电石与水反应制得的乙炔气中混杂着H2S、PH3等杂质气体,其还原性比乙炔强,是H2S、PH3使上述两种溶液迅速退色,并非乙炔发生了反应,但是却给学生一个实验成功的假象;硫化氢、磷化氢等杂质,这些既有毒又有臭味气体弥散在教室里,很长时间才能消除。
介绍一种制取纯净乙炔的新方法:
1 准备 (如下图所示)
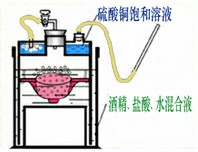
向《沉浮式气体发生器》容器里加300mL 50%浓度的酒精水溶液和盐酸的混合液,向气罩顶部的配重盒里加100ml饱和硫酸铜溶液,用乳胶管把活塞导管和配重盒上的导管连接起来,反应胆里放适量电石,悬挂在气罩内壁U 形槽里,而后把气罩插入容器里。
2 实验步骤
打开活塞导管,气罩下沉,电石和混合液接触发生反应,含杂质的乙炔气穿过硫酸铜溶液,经洗涤净化后从导管排放出来,待气罩内里的空气排净后(要做纯度检验),即可使用纯净无味的乙炔气做各项实验。当实验暂停时,关闭活塞导管,气罩上浮,电石和混合溶液脱离,反应自行停止。实验十分简单、方便、安全。
3 分析
3.1 酒精在混合液里的作用:酒精和电石不反应,用酒精调节水的浓度,从而降低反应速度;酒精是消泡剂,可消除反应时出现的大量泡沫。
3.2 盐酸在混合液里的作用:盐酸和电石不反应,盐酸可溶解糊状的Ca(OH)2,以保证反应随时发生随时停止。
3.3 硫酸铜溶液的作用:既是配重液(增大排出乙炔气的压强),又是洗涤液,不仅可以吸收新生成的乙炔气里混杂的H2S、PH3气体,还可以吸收乙炔气里混杂的酒精蒸气、氯化氢气体,从而得到纯净的乙炔气,这才符合实验的真实性和科学性。
▲ 探究实验设想提示
甲烷、乙烯、乙炔在空气中燃烧火焰明亮程度不同,仅用"含碳的质量分数不同"能解释了的吗,与碳原子间的单键、双键、三键键能有无关系?
