离子反应的实验探究 |
|
|
| 来源:不详 更新时间:2013-4-17 13:23:57 |
|
|
|
|
[实验目的]通过对本实验现象的分析,探究电解质在溶液中发生反应的实质。
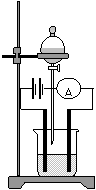
[实验准备]如右图所示,在250mL烧杯中装入约100mL稀硫酸,插入两根碳棒(从电池中自取)做电极,用两节5号电池做电源,连接一个电流计(可以用小电珠代替),再接上一个开关(未画出),将盛有稀氢氧化钡溶液的分液漏斗置于铁架台上。
[实验记录]
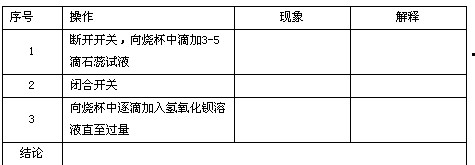
[信息检索]硫酸与Ba(OH)2所属物质类型;从酸、碱、盐电离的角度分析,稀硫酸和Ba(OH)2的水溶液中的微粒种类;电解质溶液的导电能力与自由离子浓度大小关系;石蕊在酸性、中性、碱性溶液中的一般颜色)
[思维路径]硫酸与Ba(OH)2分别属于酸、碱类的电解质→从电离的角度分析,硫酸与Ba(OH)2溶液中的所含微粒分别是H+、SO42-、Ba2+、OH-→电流计指针读数变小,溶液导电能力减弱,自由离子浓度减小,离子有消耗,参加了化学反应→溶液由红变紫,即溶液酸性减弱,证明H+和OH-结合生成了水→不难推断,白色难溶物是Ba2+与SO42-结合生成的BaSO4沉淀→稀硫酸与Ba(OH)2溶液反应的实质是溶液中的H+、SO42-、Ba2+、OH-相互结合生成了水(难电离物)和BaSO4沉淀(难溶物)→电解质溶液间的反应实质是离子间的反应。
[问题迁移]请说明下列反应的实质:NaOH溶液与CuSO4溶液的反应(如果用这两种溶液做上述实验,现象会怎样,说说你的理由)
|
上一个化学: 一氧化氮与氧气反应实验的改进探索
下一个化学: 微型化学实验设计三例 |
|
|
|
|
