�����ǿ����������ѧ��ѧ��ѧ���ص����ݡ�Ũ��ϡ�����ͭ�ķ�ӦҲ����Ҫ����ʾʵ��,�̲��е�ʵ�������:����֧�Թ��и�����һС��ͭƬ,�ֱ��������Ũ�����ϡ����,�����ô����ܵĽ�����ס�Թܿ�,������������ʢ������������Һ���Թ���,�۲�����ͭ��ϡ���ᷴӦ,�����Թ��ڴ��ڿ���,ֻ�ܹ۲쵽����ɫ����,�۲첻����ɫ���塣����,Ũ�����ͭ�ķ�Ӧ�۲쵽�����,��Ӧ���ܼ�ʱֹͣ,ֻ�ܵȵ��������ͭƬ��Ӧ��,��ɶ�ҩƷ���˷�;Ũ�����ͭ�ķ�Ӧ����,������NO2����������Ⱦ������
����
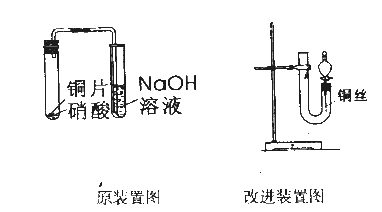
���������������,���߽����˸Ľ�,��ȡ��������Ч����ԭʵ��װ��ͼ�Ľ����ʵ��װ��ͼ����:
����
�����Ľ����ʵ�������������:
����
����(1)��Һ©���Ļ���,��U��һ��ͨ��С©��ע��ϡ����,ʹҺ��պ�������������Ϊֹ,�رշ�Һ©��������
����
����(2)��Ӧ��ʼ��,�ɹ۲쵽����ɫ�������Һ���ݳ����ۼ���ͭ˿����,�����ɵ�����ѹǿ�������ʹ����Һ���ͭ˿����Ӵ���,��Ӧ����ֹͣ��
����
����(3)��Һ©���Ļ���,��ɫ��������Һ©��,�ɹ۲쵽����ɫ���塣����װ����ע��Ũ����,��Ӧ��ʼ��,��ֱ�ӹ۲쵽����ɫ����ۼ���ͭ˿����,�ȵ�����Һ���ͭ˿����Ӵ���,��Ӧ������ֹͣ��
����
����(4)��Ӧ������,���Һ©���м���NaOH��Һ,��������ĵ��������
����
�����Ľ����ʵ��װ�õ��ŵ�:
����
����(1)װ�ü�,��������,��������,�ɹ��ʸߡ�
����
����(2)����װ��Ϊȫ���,����Ⱦ,��ȫ�ɿ���
����
����(3)��Ӧ�ɿ���,��ԼҩƷ��
|
