胆矾受热分解及硫酸铜遇水变色实验演示 |
|
|
| 来源:不详 更新时间:2013-6-20 23:23:25 |
|
|
|
|
实验仪器及药品(包括浓度)
仪器:Y形管,带铁夹的铁架台,小胶塞,酒精灯用品:一小块湿毛巾
药品:胆矾硫酸铜(其质量比约大于25:16)
实验装置图
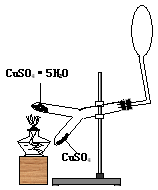
实验步骤
1、在Y形管两侧内管内分别装适量的胆矾和硫酸铜粉末,注意观察药品的颜色。
2、在试管颈部裹一块湿毛巾布(目的是冷却水蒸气,减少其散失到空气中)。
3、在管口带上一个拴有气球的单孔胶塞(起到缓冲作用)。
4、固定试管(试管口向上倾斜,盛晶体的支管口微向下倾斜,盛硫酸铜的支管微向上倾斜,便于液体回流)
5、先加热胆矾支管,观察发生的现象;再加热另一支管,观察发生的现象。如此可以反复操作。
实验注意事项
胆矾和硫酸铜的量要适合。
药品要平铺在两侧管壁上。
Y形管倾斜度要适度(冷凝水恰好流下为准)。
单孔塞的玻璃导管略长些,且塞外导管成90度(一是利于空气冷凝,二是利于气体回流)。
教法说明:
胆矾受热分解是在教材第十章第一节的一个实验,而其分解的产物之一的硫酸铜遇水的反应却在第一章第一节“学生实验”中粗略的接触过,这本是关系十分密切的两个实验,却把他们生硬的拆开,而且两个知识点放的位置特别远,不利于同学掌握。再有,在综合实验中,利用硫酸铜遇水由白色变成蓝色的明显现象,可以检验“水”的存在,补做此实验,有它的重要性和必要性。另外,硫酸铜与水恰好完全反应时,所需水量不宜控制。为此,我将两个实验利用Y形管的特点,控制胆矾和硫酸铜的用量(略大于25:16)来进行此实验,效果甚佳。其优点有:1、硫酸铜晶体能分解出水,及硫酸铜又能与生成的水化合,水得到再次利用且适量。
2、通过颜色明显变化,直观体现了两实验间的关系;同时说明了硫酸铜能够检验“水”的存在。使学生印象更深,为以后综合实验题做准备。
3、药品能做到几个班重复使用,节约药品。
4、操作简便可行。
5、有一定的趣味性。
|
上一个化学: 多采多姿的铜离子化学游戏
下一个化学: 白磷燃烧的实验改进 |
|
|
|
|
|
|
