氮气的实验室制备 |
|
|
| 来源:不详 更新时间:2013-7-11 17:22:15 |
|
|
|
|
1、实验方法
方法(一)
实验装置如图所示
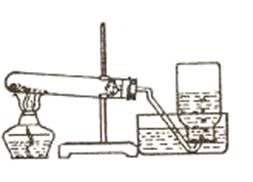
(1)将重铬酸铵放入试管内,试管口堵一点棉花,塞好带导管的单孔胶塞。
(2)用酒精灯加热盛重铬酸铵的试管底部,可观察到试管内有火花出现(无危险),随即便有绿色的三氧化二铬生成,同时有氮气放出。
(3)用排水集气法收集氮气,备用。
实验说明
(1)有关化学反应方程式:
(NH4)2Cr2O7===Cr2O3+3H2O+N2↑(加热)
(2)重铬酸铵要用细颗粒,大约1g-2g,在试管内薄薄地铺一层。否则放出的氮气太快,会使单孔胶塞冲出。
(3)生成的三氧化二铬应加以保留,作为某些化学反应(如氮的氧化)的催化剂。
方法二
实验装置如图所示。
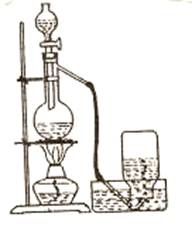
(1)往烧瓶内注入30ml氯化铵饱和溶液,向分液漏斗加入30ml亚硝酸钠饱和溶液。
(2)用酒精灯加热烧瓶,待烧瓶内溶液开始冒泡时(85℃左右)停止加热。
(3)逐滴加入亚硝酸钠饱和溶液。当空气排尽之后,用排水取气法,收集氮气。
实验说明
(1)实验原理:
NH4Cl+NaNO2=====NaCl+NH4NO2(加热)
NH4NO2=====2H2O+N2↑(加热)
(2)实验室制备纯净氮气,可用加热分解亚硝酸铵的方法。但亚硝酸铵不易保存,所以一般都通过氯化铵和亚硝酸钠反应来制备。
(3)氯化铵饱和溶液的制备:室温(25。C),在100g水中,溶解40g氯化铵,即可制成饱和溶液。
亚硝酸钠和溶液的制备:室温(25。C)在100g水中,溶解90g亚硝酸钠,即可制成饱和溶液。
(4)因为氯化铵和亚硝酸钠反应是放热反应,所以加热至85。C左右停止加热,以后可由反应放出的热量维持反应的正常进行。
(5)通过滴加亚硝酸钠饱和溶液,来调节氮气生成的速度。如果反应太剧烈,溶液产生大量泡沫,使溶液的液面上升,这时应马上用湿布包住烧瓶进行降温,以免液体冲出。
用制备的氮气,让学生进行观察,由学生自己讲述氮气的物理性质。讲授氮气的化学性质时,可以让学生将点燃的火柴放进氮气瓶中,观察;也可将镁带点燃,放入氮气瓶中,进行观察。由以上两个实验说明,所谓支持燃烧与不支持燃烧的说法只是相对的道理。
|
上一个化学: 过氧化钠与二氧化碳反应(演示实验改进)
下一个化学: 简法充氢气球 |
|
|
|
|
