��������ķֽⷴӦ |
|
|
| ��Դ������ ����ʱ�䣺2013-7-19 16:09:35 |
|
|
|
|
һ��ʵ��Ŀ�ģ���ѧ����һ���˽��������Ļ�ѧ���ʡ�
����
��������ʵ�鲽�裺
����
����1��ȡһ��125mL֮��ƿ����ƿ����
����
����2������30-50mL��30������������Һ������ƿ�ڡ�
����
����3����Լ2g�ĵ⻯�ع�����װ�����ڣ�С�ĵؽ�������ڷ������ͼһ��ʾ��
����
����4��������֮�����������ƿ֮ƿ��������ƿ������������ʹ����������գ���ͼ����ʾ��
����
����5��ȡ�������ò���������������Һ�У��漴�������������������������ھ��˳���ʱ֮Ч������ͼ����ͼ����ʾ��
����
������������ʵ��ԭ������ص����⣺
����
����1�����ʵ��ǣ�浽����������Һ�ķֽⷴӦ������������ˮ�������ܷ�ӦʽΪ��
����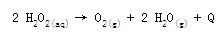
����2�����ʵ�����������У���IO��Ϊ��Ӧ���м����ʡ�
����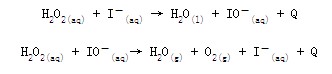
����3�����������ڳ�̬�·ֽ����ʲ��죬����⻯�غ�ƿ�����������������ã���������������ˮ������ʾ�⻯���ڷ�Ӧ�з����˴����á�
����
����4�����ʵ���������Ĵ���������ʲô�������ʵ���������Ĵ����������ɹ�������ֽ���������������ˮ��������
����
����5�����������ʿ��Դ���⻯�ز����������ֽⷴӦ�𣿣�����ʹ�ö������̴���⻯����Ϊ��������ֽⷴӦ�Ĵ�������
����
�����ġ�ע�����
����
����1����ʹ�ù����MnO2��������KI��������������ķֽⷴӦ��
����
����2��ʵ������H2O2ǰ��Ӧ���������Ա���Ƥ���Ӵ���H2O2��������ˡ�
����
����3����ʦ����ʾǰ��������Ԥ������ȷ����Ӧ��������������״ˮ����֮Ч����ȷ����H2O2Ũ����KI֮������(ע�⣺H2O2Ũ�ȹ���ʹ��Ӧ���ڼ��Ҷ�˲���������������ˮ�������)
|
��һ����ѧ�� þ�ڵ�����ȼ��
��һ����ѧ�� û���� |
|
|
|
|
