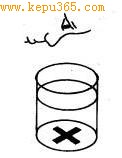
――盐酸与硫代硫酸钠的反应
【实验原理】
na2s2o3(aq)+2hcl(稀)so2(g)+s(s)+2nacl(aq)+h2o
反应缓慢生成不溶于水的硫;使溶液出现乳白色浑浊,通过观察溶液的浊度来估测反应速率。改变硫代硫酸钠的浓度而保持盐酸的浓度不变,通过测定溶液达到同等浊度时所需的时间来比较反应物浓度对反应速率的影响。
【实验步骤及现象】
将8g硫代硫酸钠溶解在200ml蒸馏水中配制成溶液。如下图所示,取50ml配好的硫代硫酸钠溶液倒入100ml烧杯中,将烧杯放在画有黑色十字的纸上,向烧杯中加入5ml2mol/l的盐酸,立即开始记时,边搅拌边从溶液上方观察溶液的浊度,透过浑浊的硫,当看不见黑色十字时,记录时间。
分别将30ml、20ml、10ml配制好的硫代硫酸钠溶液用蒸馏水稀释至50ml,保持盐酸浓度不变,重复以上操作,随着硫代硫酸钠溶液稀释程度的加大,看不到黑色十字的时间变长,这表明反应物的浓度越小,反应所需时间越长(反应速率越小)。以硫代硫酸钠溶液中溶质的浓度对时间作图。