为什么水在4度时密度最大? |
|
|
| 来源:不详 更新时间:2013-5-22 19:06:27 |
|
|
|
|
温度改变时,水的体积变化也不寻常,它在0-4℃范围内,一反“热胀冷缩”的普通规律,而是在4℃时密度最大,高于或低于此温度时,密度都较小,因此当水结冰时,体积反而大而变轻,所以冰浮在水面上。水的这一特性,对自然界水下生命的保护有着十分重要的意义,当冬季河流、湖泊冰封水面时,反而保护了水下生物的生存。
水的特殊的理化性质,是与水分子的极性分不开的。在H2O的分子中,两个O―H键间的键角为104.5°,因此H2O分子是一个极性分子。由于氢键的存在,冰和水具有很多不寻常的性质。H2O分子中每个氢原子都参与形成氢键,使H2O分子之间构成一个四面体型的骨架结构。每一个氧原子周围有4个氢原子,其中2个H是与O共价结合,另外2个H离得稍远,通过氢键与O键合,由此形成一个有很多“空洞”的结构,从而使冰的密度小于水,所以水浮于水面。当冰在冰点溶化时,部分氢键被破坏,冰的骨架结构总体崩溃而变成水,但这时液态水中仍有大量氢键存在。
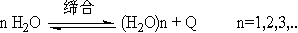
温度升高,上述平衡向吸热方向移动,即向左移动,缔合程度减少,在到达水的沸点时只有少数的缔合水分子。温度降低,平衡右移,水的缔合作用增大。水在4℃时的缔合作用最大,即此温度下,这些H2O分子堆积最紧密,此时水摩尔体积最小,故密度最大。破坏水分子的缔合结构时,要消耗较多的能量,故冰熔化热、熔点、水的比热、沸点及汽化热等性质和同族其他元素的氢化物相比,都高得多。
|
上一个化学: 中考10门课 学生减负还需再给力!
下一个化学: 浅谈初中化学复习课趣味教学方法 |
|
|
|
|
